亲核加成反应

 Clash Royale CLAN TAG#URR8PPP
Clash Royale CLAN TAG#URR8PPP 
一个亲核加成反应的例子:酮羰基被羟基化合物在碱性条件下加成,形成了半缩酮。
有机化学中,亲核加成(Nucleophilic addition)是反应物的π键受亲核试剂进攻而被取代,形成两个新的共价键。[1]
加成反应局限于以下一些含多重键的底物:
- 含碳-杂原子多重键:羰基化合物、亚胺或腈。
- 含碳-碳多重键:烯烃、炔烃及衍生物。
目录
1 碳-杂多重键的加成
1.1 对羰基的加成
1.2 对腈的加成
1.3 对亚胺和其他底物的加成
2 对碳-碳双键的加成
3 参考文献
4 参见
碳-杂多重键的加成
对于碳-杂原子多重键例如 C=O 或者 CN 的亲核加成反应在有机化学当中相当广泛。这些化学键都是具有极性的(在两个成键原子之间有较大的电负性差异),而通常结果是碳原子会因较低的电负性而带部分正电荷,这就导致了碳原子成为主要的亲核加成反应进攻位点。
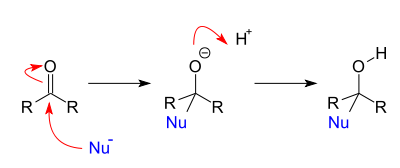
对羰基的亲核加成
这种反应类型也称为1,2亲核加成反应。此类亲核进攻在没有其他控制因素影响下(例如存在路易斯酸和螯合剂)不会造成立体化学问题,得到的都是消旋产物。加成反应的种类很多,当加成反应还伴有消除反应称为亲核酰基取代或者加成-消除反应。
对羰基的加成
当羰基是亲电试剂,亲核试剂可以是:
- 与水在水解反应中生成偕二醇(水合物)。
- 与醇在缩醛化反应中生成缩醛或缩酮。
- 与有机氢化物在有机还原反应中得到醇。
- 与胺、甲醛和一个羰基化合物发生曼尼希反应。
- 与烯醇发生羟醛缩合或者Baylis-Hillman反应。
- 与有机金属亲核试剂发生格氏反应、Reformatsky反应或者Barbier反应。
- 与叶立德比如维蒂希试剂、Corey-Chaykovsky试剂或者α-硅负离子Peterson烯烃合成发生反应。
- 与膦负离子反应:Horner-Wadsworth-Emmons反应。
- 与吡啶两性离子反应:Hammick反应。
- 与乙炔发生反应:Favorskii反应。
对腈的加成
当腈是亲电试剂,亲核加成出现于下列反应:
- 腈的水解,生成酰胺或羧酸。
- 与有机锌试剂发生Blaise反应。
- 与醇发生Pinner反应。
- 两分子腈发生Thorpe反应生成烯胺,分子内反应称为Thorpe-Ziegler反应。
对亚胺和其他底物的加成
- 利用氢化物对于亚胺的加成制备胺:Eschweiler-Clarke反应。
- 利用水对于硝基烷烃的加成制备羰基化合物:Nef反应。
- 利用醇对亚胺加成后生成异氰酸酯,制备氨基甲酸酯。
亲核试剂通过一个特定的角度进攻羰基碳正中心,被称为Bürgi-Dunitz角。
对碳-碳双键的加成
对于烯烃加成的驱动力在于亲核试剂X-和一个缺电子不饱和双键形成共价键(第一步)。在X上的负电荷被转移到了碳-碳键上。

对烯烃的亲核加成
第二步,带有负电荷的碳负离子结合缺电子的(Y)形成共价键。
一般的烯烃不易受到亲核进攻的影响,因为碳碳双键不具有碳氧双键那样较强的极性。但如果双键所在碳上连有比较强的吸电子基团或共轭体系,则有利于反应的发生,比如阴离子聚合反应的引发步骤,和苯乙烯在甲苯中和钠反应得到1,3-二苯基丙烷。
[2]就是通过这种碳负中间体:

苯乙烯在甲苯中与钠反应
有个例外在Varrentrapp反应中发现。富勒烯具有不寻常的双键活性和加成活性,比如Bingel反应。
当X是一个羰基比如 C=O 或 COOR 或是一个氰基 CN,反应类型就是共轭加成反应。这里的取代基X能够通过诱导效应帮助稳定碳原子上的负电荷。
当Y-Z是一个含有活性氢的化合物(易去除一个氢原子形成碳负中间体),反应就是熟知的Michael加成反应。
全氟烯烃(烯烃的所有氢原子被氟原子取代)非常倾向于进行亲核加成反应。
参考文献
^ March Jerry; (1985). Advanced Organic Chemistry reactions, mechanisms and structure (3rd ed.). New York: John Wiley & Sons, inc. ISBN 0-471-85472-7
^ Sodium-catalyzed Side Chain Aralkylation of Alkylbenzenes with Styrene Herman Pines, Dieter Wunderlich J. Am. Chem. Soc.; 1958; 80(22)6001-6004. doi:10.1021/ja01555a029
参见
- 亲核取代反应
- 亲电加成反应
- 伯基-丹尼兹轨道
| ||||||||||||||||||||||
|


